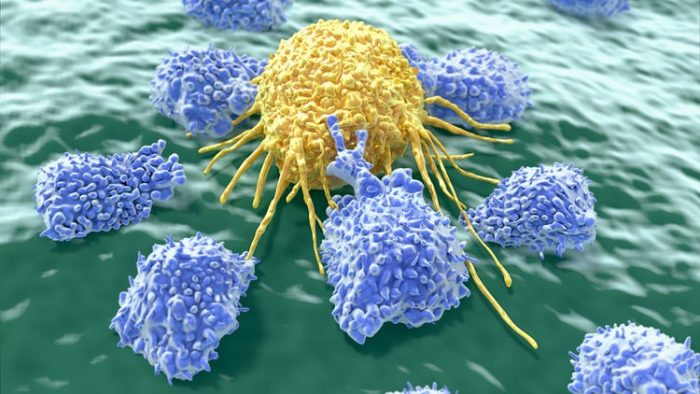
El sistema immune s’encarrega d’eliminar tot allò estrany per al nostre organisme, com virus o bactèries. Està format per tipus cel·lulars especialitzats. Els limfòcits B detecten directament estructures estranyes amb anticossos (Ab de “Antibody”) que després secreten per neutralitzar-les. Els macròfags mengen microbis i els digereixen per exposar a la seva membrana petits fragments de les proteïnes unides al complex major d’histocompatibilitat (MHC). Els limfòcits T reconeixen aquests petits fragments amb un receptor especial (el TcR de “T-cell receptor”) i s’activen per matar altres cèl·lules infectades que presentin els mateixos fragments.
Les proteïnes o altres molècules detectades pels Ab o els TcRs s’anomenen antígens (Ag) i el petit fragment detectat s’anomena epítop. Un procés especialitzat de recombinació gènica que ocorre en el moll d’ós i el timus genera un gran repertori de limfòcits amb Abs o TcRs diferents; per altre banda, els limfòcits que reconeixen molècules o proteïnes pròpies són eliminats. Així, els limfòcits en circulació perifèrica poden reconèixer qualsevol proteïna que no té una seqüencia normal o pròpia de l’individu.
El càncer es genera com a conseqüència de mutacions en l’ADN que activen la proliferació incontrolada de les cèl·lules. Hi ha factors ambientals que contribueixen a generar aquestes mutacions, com la radiació ultraviolada del sol o el tabac. Aquestes mutacions generen proteïnes mutades amb funcions alterades. Per exemple, es perd la funció de proteïnes que frenen la divisió cel·lular o que controlen la mort cel·lular; o be s’activen proteïnes que estimulen la divisió cel·lular. A més, les mutacions poden afectar a les proteïnes reparadores dels errors de còpia de l’ADN durant la divisió cel·lular i, en aquest cas, el nombre de mutacions augmenta. El conjunt de mutacions del tumor s´anomena “mutanoma” i noves tècniques de seqüenciació permeten determinar-lo en pocs dies a partir d’una biòpsia del tumor.
Algunes proteïnes mutades del tumor són reconegudes com antígens i el sistema immune elimina constantment cèl·lules tumorals. Sense sistema immune els tumors serien molt més freqüents. Eventualment però, les mutacions poden afectar a proteïnes que regulen el propi sistema immune i, així, la cèl·lula tumoral adquireix la capacitat d´inhibir el sistema immune. S´estableix un equilibri entre el sistema immune i el tumor que pot durar anys. Però la cèl·lula tumoral en equilibri és potencialment molt perillosa per la seva capacitat de divisió permanent i de generar noves mutacions que li confereixin una major habilitat d’adaptació a la pressió de l’entorn. Així, en comptades ocasions, aquesta adaptació culmina amb un cèl·lula que evadeix el sistema immune i el càncer progressa de forma incontrolada.
La immunoteràpia del càncer es relativament “antiga”. A finals del segle XIX, William Coley va injectar bacteris dins dels tumors per promoure la resposta immune. Aquest tipus d’immunoteràpia va esdevenir una realitat clínica a partir de 1976, quan el bacil de Calmette-Guerin, que s’usava com a vacuna per a la tuberculosi, es va utilitzar per tractar el càncer de bufeta. Els virus també van ser usats en els anys 70s per activar el sistema immune dins dels tumors. Però la revolució de la immunoteràpia en el tractament del càncer és recent i lligada al coneixement dels múltiples mecanismes que el tumor utilitza per evadir el sistema immune. Per exemple la cèl·lula tumoral pot perdre la capacitat de presentar antígens o produir proteïnes que inhibeixen els limfòcits.
L’any 1995, James Allison va descobrir que la proteïna CTLA4 de la membrana dels limfòcits T actuava com un inhibidor de la activació d’aquestes cèl·lules perquè les respostes immunes no acabessin fora de control en condicions normals. Aquests receptors s’anomenen “inhibidors de punts de control” o, de l’anglès, “checkpoint inhibitors”. James Allison va descriure que els tumors usen CTLA4 per evadir el sistema immune i, així, bloquejant la funció de CTLA4 amb un anticòs els tumors podien ser rebutjats. L’any 2000 es va iniciar el primer assaig clínic amb l’anticòs anti-CTLA4 Ipilimumab; el 20% dels pacients que van tractar-se llavors encara estan vius avui en dia, 20 anys després. L’any 2011, Ipilimumab va ser aprovat contra el melanoma. James Allison va ser estat guardonat amb el premi Nobel de Fisiologia o Medicina 2018.
Un altre “checkpoint inhibitor” és el PDL1 que s´uneix al PD1 dels limfòcits T. Aquesta inhibició va ser descoberta per Tasuku Honjo l’any 1992 i, per això, va compartir el premi Nobel 2018 amb James Allison. Els tumors poden expressar PDL1 per a inhibir els limfòcits T. L’any 2014 es va aprovar l’ús comercial del anticòs anti-PD1 Nivolumab per a melanoma cutani i, més tard, per al càncer de pulmó, ronyó, fetge, colon, recte i limfoma. Un altre anti-PD1 aprovat per melanoma, càncer de pulmó, cèrvix, estómac, limfomes, i altres tumors és el Pembrolizumab. Els anti-PDL1 també han resultat eficaços; com el Atezolizumab en bufeta, el Avelumab en carcinoma de Merkel, o el Durvalumab en bufeta i pulmó.
Els resultats descrits han revolucionat el tractament de molts tipus de càncer, sobretot d’aquells que presenten més mutacions i, per tant, més antígens, com són el melanoma cutani associat a les mutacions induïdes pel sol, o el càncer de pulmó associat al tabac. A més, l’èxit dels inhibidors de “checkpoint inhibitors” ha esperonat altres tipus de immunoteràpies, com els agents activadors de perill pel sistema immune, les vacunes o la transferència de limfòcits que reconeixen antígens tumorals. Així s´està investigant l’ús d’agents activadors dels receptors de perill pel sistema immune com els “Toll-like receptors” i STING (estimulador dels gens de interferó). També s´està investigant quins són els antígens tumorals detectats pel sistema immune per utilitzar-los com a vacunes. Com aquests antígens son diferents per a cada tumor, aquestes vacunes són “personalitzades”, el que implica un repte en el seu desenvolupament. Finalment, es poden aïllar els limfòcits que reconeixen els antígens tumorals i multiplicar-los al laboratori. Aquest limfòcits es re-administren al pacient en una dosi que sobrepassa els mecanismes d’inhibició del tumor. Una variant d’aquesta estratègia és identificar el TcR que reconeix l’antigen tumoral i transferir el gen d’aquest TcR als limfòcits del pacient. Inclús s’ha desenvolupat un receptor artificial que pot substituir el TcR, anomenat receptor quimèric d’antigen (CAR, de “Chimeric Antigen Receptor”) basat en un anticòs que reconeix l’antigen. Així, els limfòcits T modificats amb un CAR que reconeix l’antigen CD19 expressat per limfòcits B han estat aprovats a l’any 2017 pel tractament de leucèmies i limfomes B.
Malgrat els avenços, molts malalts no responen als “checkpoint inhibitors” i altres immunoteràpies, o bé presenten toxicitats greus associades a l’activació del sistema immune. Cal molta més recerca bàsica, traslacional i clínica per augmentar l’ eficàcia de la immunoteràpia del càncer. En aquest sentit, la inversió en projectes i assajos clínics d’immunoteràpia ha crescut considerablement en els darrers anys. L’Institut Català d’Oncologia té nombrosos projectes de recerca en aquest nou camp terapèutic i ha creat una unitat especialitzada en aquest camp. S´estan estudiant nous fàrmacs dirigits contra “checkpoint inhibitors”, noves combinacions de fàrmacs en nous tipus tumorals o grups de pacients, analitzant les característiques dels tumors que responen o no als tractaments per tal de trobar marcadors predictius de la resposta, i dissenyant i desenvolupant nous agents immuno-estimuladors. En conjunt, pretenem que l’esforç de recerca en diferents àmbits contribueixi a la millora del la cura del càncer en la població general.
Ramón Alemany
Grup d’Immunoteràpia i Viroteràpia del Càncer, ProCure and Oncobell Programs. Institut Català d’Oncologia i Institut d’Investigació Biomèdica de Bellvitge